In un precedente articolo è stato mostrato che il termine elettrostatico dell’energia reticolare di un cristallo contiene un fattore (A) che dipende dal tipo di reticolo cristallino. Ora esamineremo più in dettaglio come calcolare questo termine e il suo valore per un semplice sistema ionico.
L’energia potenziale totale di un cristallo ionico è uguale alla somma dei contributi di interazione elettrostatica del tipo
degli ioni (A,B) di carica e
(con
il valore dell’unita’ di carica elettronica e
la carica netta dello ione) separati dalla distanza
.
La somma è estesa a tutte le coppie di ioni presenti nel solido per qualsiasi struttura cristallina. La sommatoria cosi definita converge molto lentamente. Infatti se l’atomo centrale considerato è positivo, i primi vicini contribuiranno con un termine negativo rilevante, i secondi vicini con un termine positivo (repulsivo) solo leggermente più piccolo, e così via. In questo modo l’effetto complessivo della somma farà in modo che l’attrazione fra i cationi e gli anioni predomina e fornisce un contributo favorevole (negativo) all’energia del solido. Vediamo oro in dettaglio come questa somma viene calcolata nel caso di configurazioni reticolari semplici.
Reticolo monodimensionale Infinito.
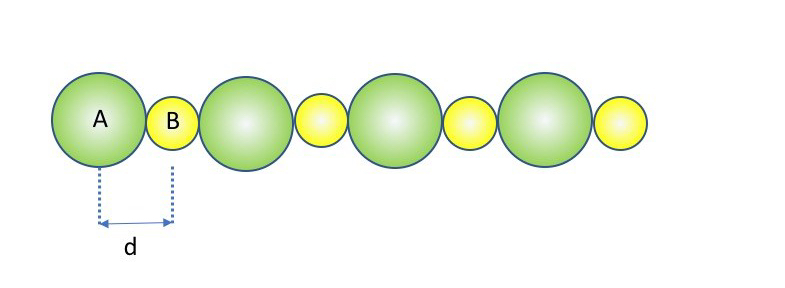
In un reticolo unidimensionale con i cationi e gli anioni alternati a intervalli costanti di lunghezza d, e con e
, l’energia potenziale d’interazione di uno ione con tutti gli altri è proporzionale a una serie del tipo:
(Il fattore 2 deriva dal fatto che ad entrambi i lati dello ione centrale ci sono ioni uguali). La somma dipende solo dal tipo di reticolo e da un parametro di scala (periodo) che è la distanza fra i centri delle particelle adiacenti, :
Nel caso monodimensionale, il potenziale V contiene un fattore specifico della carica degli ioni e della scala del reticolo, , e il fattore 2ln 2 (= 1.3862944), chiamato costante di Madelung (A), che caratterizza la simmetria del reticolo.
Il reticolo monodimensionali sono e’ un modello ideale, recentemente, infatti, e’ stata ottenuta la struttura di un cristallo monodimensionale di di sali del sodio all’interno di un nanotubo di carbonio.
Reticolo bidimensionale Infinito.
In un reticolo bidimensionale con i cationi e gli anioni sono disposti ai vertici di quadrati contigui a intervalli costanti di lunghezza d, e con e
. In Figura 2, considerando lo ione centrale (1) e muovendosi radialmente da questo, l’interazione di questo ione con tutti gli altri è proporzionale a una serie del tipo:

Reticolo Tridimensionale Infinito.
Questi risultati si possono estendere a reticoli tridimensionali. Nei solidi semplici la costante di Madelung è specifica del tipo di cristallo e indipendente dalle distanze interioniche.
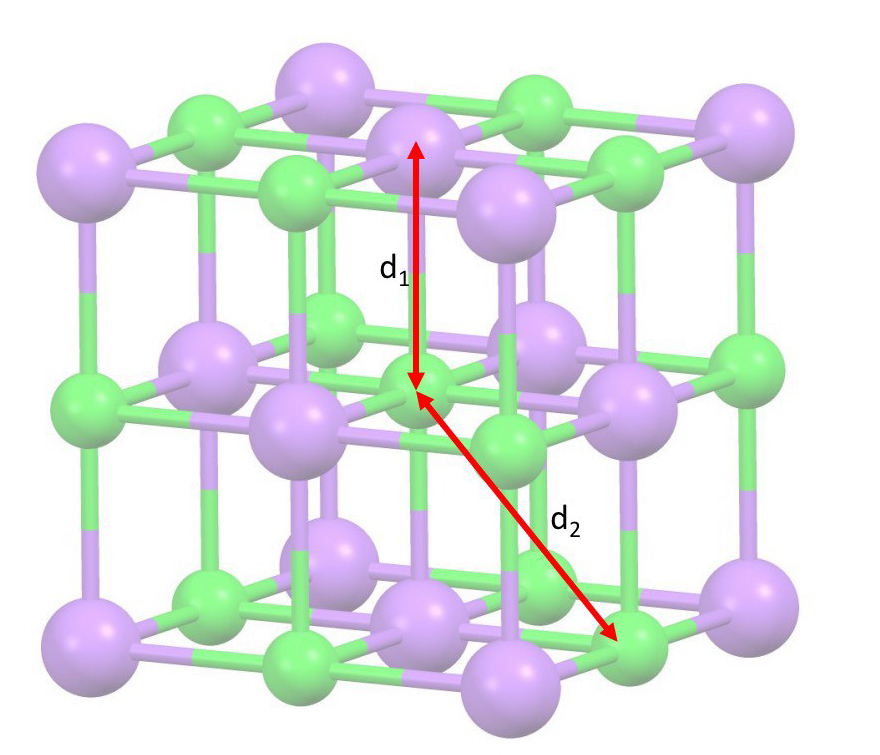
Per calcolare la costante di Madelung per un reticolo tridimensionale si può procedere in questo modo. Partendo da un opportuno ione collocato al centro della nostra porzione di reticolo (Figura 3), ci allontaniamo radialmente fino ai primi vicini, che saranno di carica opposta, di numero pari a e posti a una distanza
. Procedendo arriviamo ai secondi vicini (più lontani e di carica uguale), in numero di
, e a una distanza
, e così via. La costante di Madelung si potrá quindi esprimere con questa sommatoria estesa all’infinito:
dove indica che il segno di ogni termine della sommatoria è positiva se gli ioni hanno carica opposta (attrazione) e negativa se hanno uguale carica (repulsione);
è la scala del reticolo (somma dei raggi ionici
+
).
Consideriamo uno ione Na in NaCl, ad esempio, esso ha 6 primi vicini Cl-(n
= 6) a distanza
; vi sono poi 12 secondi vicini Na
(
) a distanza
; vi sono poi 8 terzi vicini Cl
(
) a distanza
ecc. Avremo allora la serie:
L’energia potenziale totale per mole di unità di formula in una struttura cristallina arbitraria è:
| Struttura | A | A/n* | Coordination |
| Cloruro di Cesio (CsCl) | 1.763 | 0.88 | (8,8) |
| Salgemma (NaCl) | 1.748 | 0.87 | (6,6) |
| Fluorite (CaF | 2.519 | 0.84 | (8,4) |
| Solfuro di Zinco o Wurtzite (ZnS) | 1.641 | 0.82 | (4,4) |
| Cloruro di Cadmio (CdCl | 2.244 | 0.75 | (6,3) |
| Ioduro di Cadmio (CdI | 2.191 | 0.73 | (6,3) |
| Ossido di Alluminio o Curundum ( | 4.172 | 0.83 | (6,4) |
| Diossido di titanio o Rutile ( | 2.408 | 0.80 | (6,3) |
La costante di Madelung cresce con l’aumentare del numero di coordinazione. Infatti il contributo più rilevante deriva dai primi vicini. I valori per la struttura NaCl (6,6) e per quella tipo CsCl (8,8) illustrano l’andamento.

Pingback: Madelung常数的计算 |
Pingback: Madelung定数の計算 |
Pingback: El cálculo de la constante de Madelung |