Quest’anno ricorre l’anniversario della pubblicazione dell’articolo di Edwin Schrödinger (1887-1961) in cui viene introdotta la sua famosa equazione. Prendendo spunto da questa occasione, ho ripescato e rinnovato uno dei miei antichi progetti di programmazione in BASIC con i miei microcomputer negli anni ’80. Di nuovo il microcomputer era il mio amato Phillips MSX, di cui ho parlato in altri blog. Studiando chimica, non potevo non essere attratto dalla bellezza e dall’eleganza delle soluzioni dell’equazione di Schrödinger per l’atomo d’idrogeno. Inspirato dal libro (S. Marseglia, La Chimica col personal computer pubblicato dalla Muzzio) in cui mostrava alcuni esempi di programmi in BASIC per la chimica, decisi di imbarcarmi nell’impresa e usare l’MSX e poi l’Amiga Basic Basic per provare a riprodurre le bellissime visualizzazioni degli orbitali molecolari che vedevo nei libri di chimica universitari. Ma prima di questo vediamo di tornare a contenuto dell’articolo di Schrödinger.
1926–2026: cento anni dell’equazione di Schrödinger
Il 2026 segna un anniversario particolarmente significativo per la fisica moderna: cento anni dalla formulazione dell’equazione di Schrödinger, pubblicata nel 1926. Con quel lavoro, Erwin Schrödinger fornì per la prima volta una descrizione matematica coerente e continua dei sistemi quantistici, cambiando radicalmente il modo di concepire la materia a scala atomica. Fu proprio applicando l’equazione di Schrödinger all’atomo di idrogeno che emerse una delle più profonde rivoluzioni concettuali della fisica: l’elettrone non percorre orbite definite, ma è descritto da una funzione d’onda distribuita nello spazio. Le soluzioni di questa equazione portarono naturalmente alla nascita degli orbitali atomici, un’accurata rappresentazione probabilistica degli elettroni intorno agli atomi. Nel 1926 queste idee erano profondamente astratte e difficili da visualizzare. Oggi, a distanza di un secolo, possiamo invece calcolare e rappresentare graficamente le funzioni d’onda dell’atomo di idrogeno anche con semplici programmi, riscoprendo la bellezza, l’estetica e l’importanza di quella rivoluzione scientifica. Questo anno segna anche un’altra importante data, la nascita del primo personal computer commerciale, l’Apple II, messo in commercio nel 1976.
Questo blog nasce proprio con questo spirito: celebrare il centenario della meccanica ondulatoria tornando alle radici teoriche dell’atomo di idrogeno. Un piccolo omaggio al 1926, realizzato nel 2026, per ricordare come una singola equazione abbia cambiato per sempre la nostra visione della natura. Quest’anno ricorre anche il cinquantenario del personal computer. Per questo motivo vorrei fare questa celebrazione utilizzando lo stesso linguaggio di programmazione dei primi esperimenti di visualizzazione scientifica sui primi personal computers.
L’atomo di idrogeno: il laboratorio fondamentale della meccanica quantistica
L’atomo di idrogeno è l’atomo più semplice esistente in natura: è formato da un solo protone (l’isotopo più leggero, il prozio), che costituisce il nucleo, e da un solo elettrone legato ad esso dalla forza elettrostatica. Proprio per questa semplicità, l’idrogeno ha avuto un ruolo centrale nello sviluppo della meccanica quantistica ed è ancora oggi un punto di riferimento fondamentale per comprendere la struttura della materia. Dal punto di vista classico si potrebbe immaginare l’elettrone come una particella che orbita attorno al nucleo, in modo simile a un pianeta intorno al Sole. Tuttavia, questa immagine è profondamente scorretta. La descrizione corretta dell’atomo di idrogeno emerge solo all’interno della meccanica quantistica, dove lo stato dell’elettrone è rappresentato da una funzione d’onda, soluzione dell’equazione di Schrödinger. Questa funzione d’onda non descrive una traiettoria, ma una distribuzione di probabilità: il quadrato del suo modulo indica la probabilità di trovare l’elettrone in una certa regione dello spazio. Le regioni di spazio in cui questa probabilità è maggiore prendono il nome di orbitali atomici.
Gli orbitali dell’idrogeno sono caratterizzati da tre numeri quantici:
- il numero quantico principale n, che determina l’energia e la dimensione dell’orbitale;
- il numero quantico orbitale l, che ne determina la forma;
- il numero quantico magnetico m, che ne determina l’orientazione nello spazio.
A seconda dei valori di questi numeri quantici si ottengono orbitali con forme molto diverse: sferiche (orbitali s), bilobate (p), a quattro lobi (d) o ancora più complesse (f). Una caratteristica fondamentale degli orbitali è la presenza di nodi, superfici o linee in cui la probabilità di trovare l’elettrone è esattamente nulla, una conseguenza puramente quantistica senza analoghi classici. La sezione che segue è un riassunto molto tecnico e condensato dell’equazione di Schrödinger nello stato stazionario. Se il lettore o la lettrice è interessata alla sua derivazione può lasciare un commento per stimolare un blog dedicato all’argomento. Altrimenti può consultare eccellenti testi universitari di chimica fisica che forniscono i fondamenti necessari.
Equazione di Schrödinger per l’atomo di idrogeno
L’equazione di Schrödinger stazionaria è: . La sua energia totale (cinetica più potenziale) è calcolata usando l’operatore di Hamilton (Hamiltoniana):
Poiché il potenziale dipende solo da , è naturale usare coordinate sferiche. Il Laplaciano in coordinate sferiche è:
Separazione delle variabili
Cerchiamo soluzioni nella forma:
Ovvero come prodotto di due equazioni separate che dipendono dalle coordinate angolari (parte angolare)
Le soluzioni sono le armoniche sferiche:
dove sono i polinomi di Legendre associati, l = 0,1,2,… and, m = -l,…,+l
L’altra equazione dipende dalla distanza (equazione radiale)
Che viene normalizzata usando la sostituzione: , a questa forma
dove sono polinomi di Laguerre associati,
è il raggio di Bohr, n = 1,2,3,…, l = 0,1,…,n-1.
Pertanto, le autofunzioni dell’atomo di idrogeno sono:
Esempi di orbitali atomici
Le funzioni d’onda dell’atomo di idrogeno sono normalizzate secondo
e possono essere scritte come
dove è il raggio di Bohr.
1s:
in coordinate cartesiane:
Visualizzare gli orbitali: dal formalismo matematico alle immagini
Come accennato nell’introduzione, il programma QB64 Basic che presento in questo blog è l’evoluzione di un programma in Basic per microcomputer che sviluppai durante gli anni universitari. Il programma utilizza le espressioni analitiche delle funzioni d’onda dell’atomo di idrogeno per calcolare le componenti radiale e angolare degli orbitali e ne rappresenta graficamente la distribuzione nello spazio.
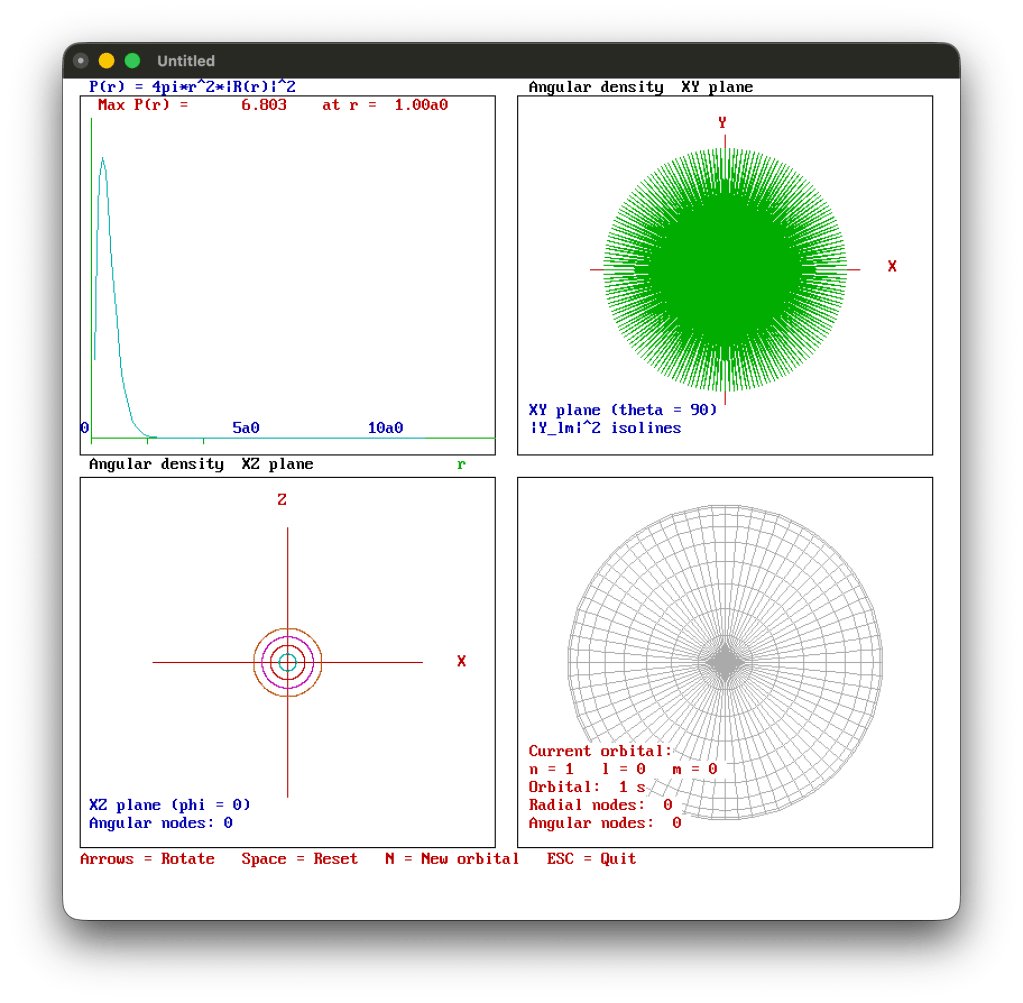
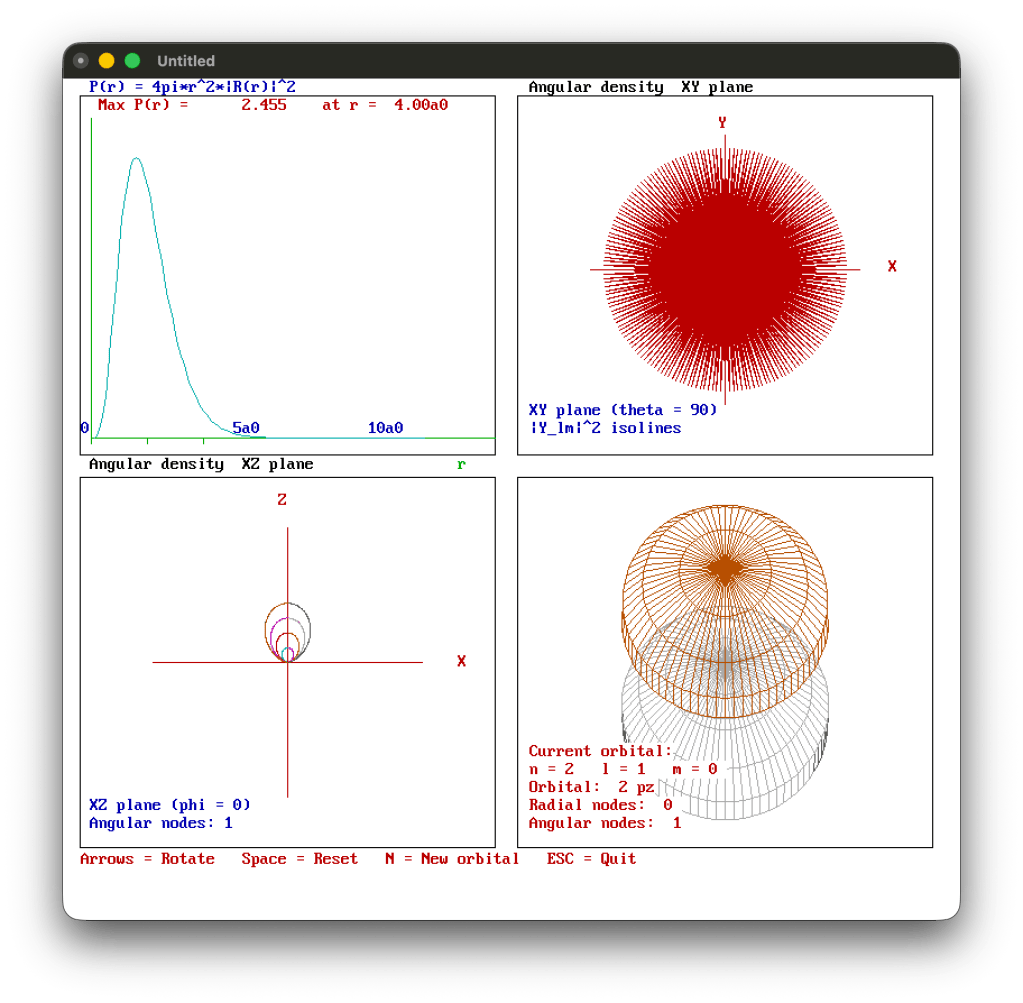
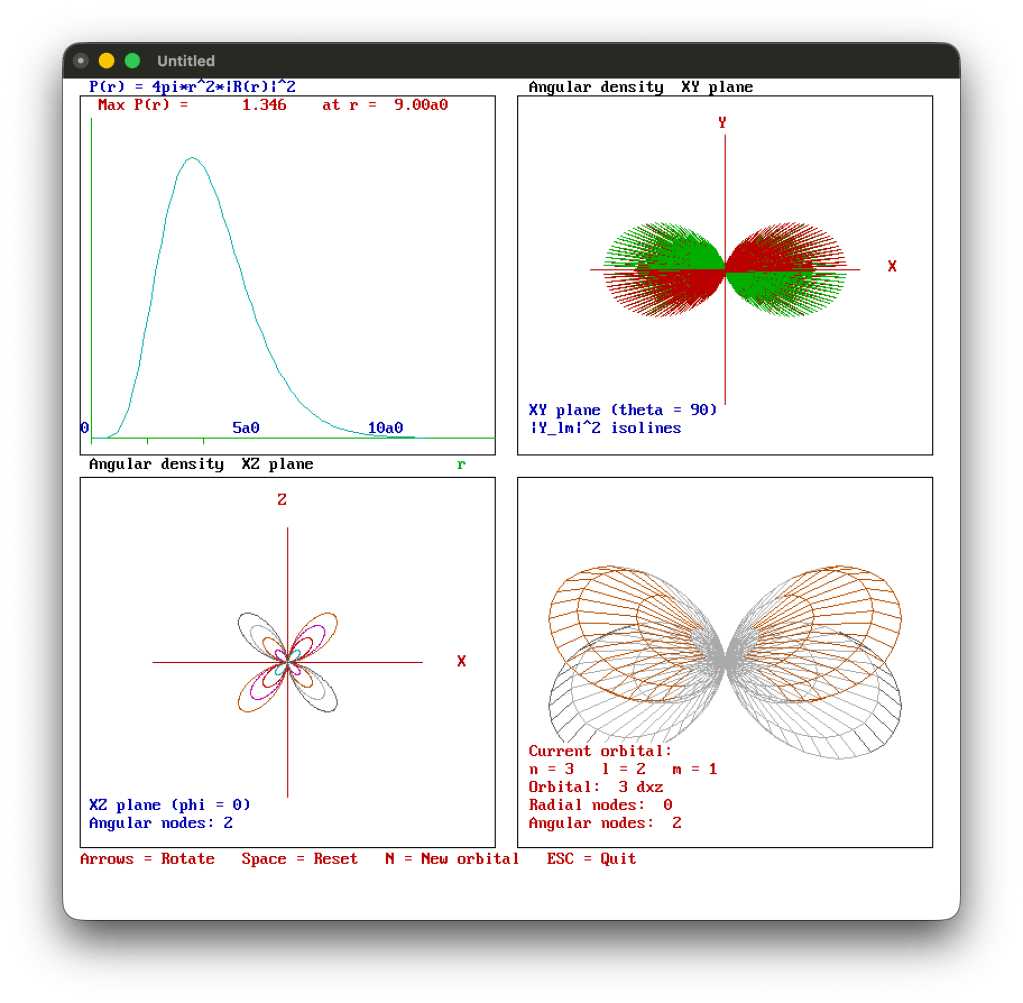
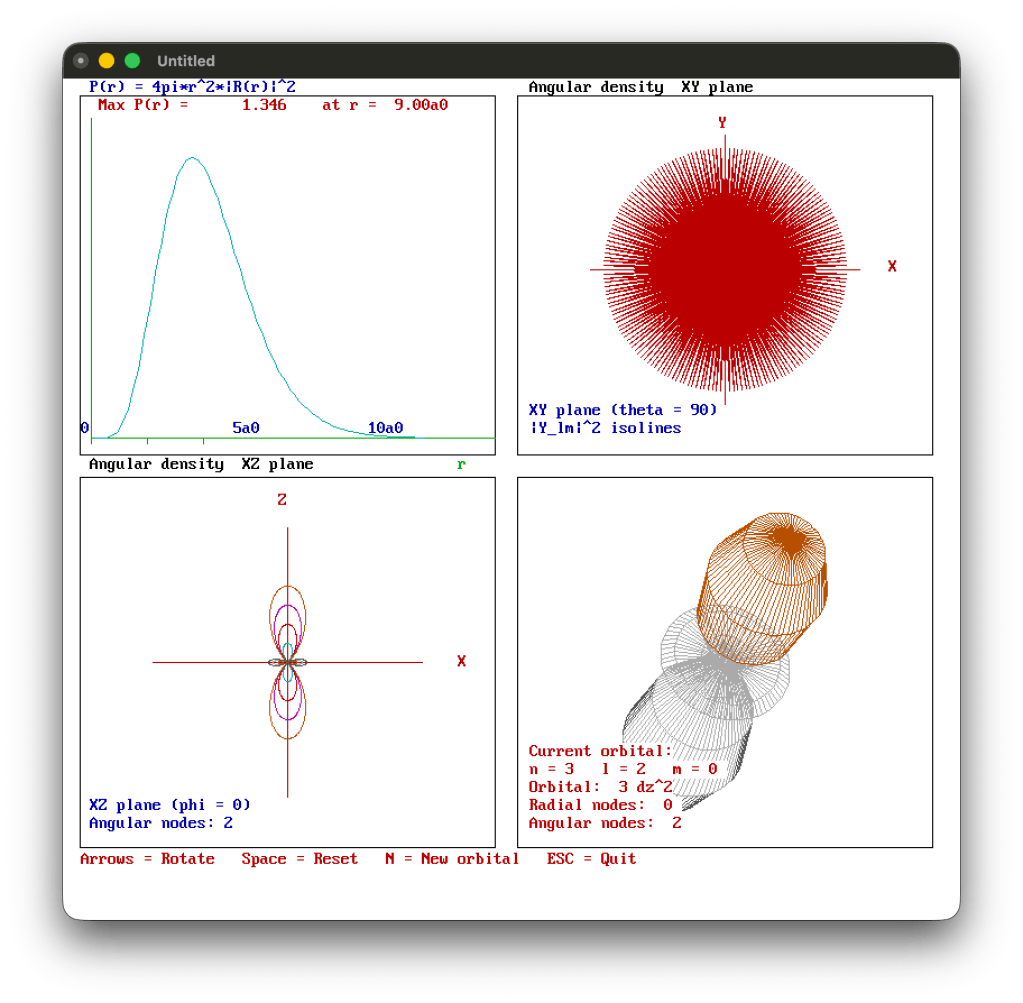
Le immagini prodotte mostrano:
- La funzione radiale (in alto a sinistra).
- la funzione angolare proiettata sul piano XZ (in basso a sinistra);
- la proiezione sul piano XY (in alto a destra);
- la rappresentazione tridimensionale dell’isosuperficie dell’orbitale (in basso a destra).
Queste rappresentazioni permettono di evidenziare
- la forma caratteristica di ciascun orbitale,
- la presenza dei nodi,
- l’orientazione nello spazio degli stati quantici.
Questo tipo di visualizzazione ha anche un valore storico e didattico. È lo stesso approccio che, a partire dagli anni Venti del Novecento, ha contribuito a rendere più intuitivo il concetto di densità elettronica, permettendo di collegare la teoria quantistica agli spettri atomici e alle proprietà chimiche degli elementi, e di comprendere meglio la struttura e la reattività di atomi e molecole.
Personalmente, la creazione di questo programma è stata un progetto molto piacevole, che mi ha aiutato a comprendere e demistificare la matematica apparentemente complessa dell’equazione di Schrödinger. Invito quindi tutti i lettori a esplorare e migliorare il programma in Appendice, magari riscrivendolo nel linguaggio di programmazione con cui hanno maggiore familiarità.
Appendice – Il programma
Seguendo una tradizione che era comune nelle riviste di microcomputer degli anni Settanta e Ottanta, riporto qui il listato completo del programma utilizzato per generare le visualizzazioni degli orbitali dell’atomo di idrogeno presentate in questo articolo. In quel periodo, riviste dedicate all’informatica personale pubblicavano frequentemente programmi completi che i lettori potevano digitare direttamente sul proprio computer per esplorarne il funzionamento e sperimentare modifiche.
Il programma presentato qui è scritto in QB64 Basic ed è l’evoluzione di un codice che avevo sviluppato durante gli anni universitari per visualizzare le soluzioni analitiche dell’equazione di Schrödinger per l’atomo di idrogeno. Il codice utilizza le espressioni esplicite delle funzioni radiali e degli armonici sferici per calcolare la distribuzione spaziale della funzione d’onda e rappresentare graficamente le caratteristiche principali degli orbitali atomici.
Le immagini generate dal programma includono:
- la funzione radiale
,
- la distribuzione angolare associata agli armonici sferici,
- proiezioni bidimensionali della densità elettronica,
- una rappresentazione tridimensionale dell’isosuperficie della funzione d’onda.
Il codice può essere utilizzato liberamente per scopi didattici. I lettori sono incoraggiati a modificarlo, esplorarne la struttura e, se lo desiderano, riscriverlo in altri linguaggi di programmazione.
Di seguito è riportato il listato completo del programma.
Nota: Il programma è fornito a scopo didattico e senza alcuna garanzia. Sebbene la versione fornita sia stata testata, l’autore non può garantire che sia priva di errori o adatta a ogni sistema.
Rem ******************************************************
Rem HYDROGENOID ORBITALS VISUALIZER
Rem QB64 Version
Rem
Rem 1926 - 2026 : 100 Years of Wave Mechanics
Rem
Rem V1.0 1987 MSX BASIC
Rem V2.0 2025-2026 Adapted for QB64 BASIC
Rem
Rem Programmed by Danilo Roccatano
Rem (c) 1987-2026
Rem
Rem This program is provided for educational purposes.
Rem ******************************************************
Screen _NewImage(800, 750, 256)
_ScreenMove 100, 50
_Display
Cls
Color 0, 15
Dim Shared PI As Double
PI = 4 * Atn(1)
a0 = 0.529 ' Bohr radius in Angstroms
ia0 = 1 / a0
Dim angY As Double
Dim angX As Double
angX = 0
angY = 0
Do
Cls
Call DrawFrames
Call WriteInfo
Color 0, 14
Locate 35, 55: Input "Enter n, l, m "; n, l, m
If n < 1 Or l < 0 Or l >= n Or Abs(m) > l Then
Locate 29, 55: Print "Invalid quantum numbers"
Locate 30, 55: Print "Press any key..."
Do: Loop Until InKey$ <> ""
Else
angY = 0
angX = 0
' -------- INTERACTIVE ROTATION LOOP --------
Do
_Limit 60
Cls
Call DrawFrames
Call WriteInfo
' ---- Rotation keys ----
If _KeyDown(19712) Then angY = angY - .05 ' Left
If _KeyDown(19200) Then angY = angY + .05 ' Right
If _KeyDown(18432) Then angX = angX + .05 ' Up
If _KeyDown(20480) Then angX = angX - .05 ' Down
' Reset view
If _KeyDown(57) Then angX = 0: angY = 0 ' Spacebar
' ---- Draw ----
Call PlotRadial(n, l)
Call PlotAngularXY(l, m)
Call PlotAngularXZ(l, m)
Call PlotAngular3DMeshHidden(l, m, angY, angX)
Call DisplayQuantumInfo(n, l, m)
Locate 44, 3: Print "Arrows = Rotate Space = Reset N = New orbital ESC = Quit"
If _KeyDown(78) Then Exit Do ' N key for new orbital
If _KeyDown(27) Then End ' ESC quits program
_Display
Loop
End If
Loop
'===========================================================
Sub DrawFrames
Line (10, 10)-(390, 340), 15, BF
Line (400, 10)-(780, 340), 15, BF
Line (10, 350)-(390, 690), 15, BF
'Line (400, 350)-(780, 690), 8, BF
Line (405, 355)-(775, 685), 7, BF
Line (15, 15)-(385, 335), 0, B
Line (405, 15)-(775, 335), 0, B
Line (15, 355)-(385, 685), 0, B
Line (405, 355)-(775, 685), 0, B
Color 0, 15
'Locate 1, 4: Print "Radial probability density"
Locate 1, 53: Print "Angular density XY plane"
Locate 22, 4: Print "Angular density XZ plane"
' Draw axes
Color 2, 15
Locate 22, 45: Print "r"
' Add scale indicators
Color 1, 15
Locate 1, 4: Print "P(r) = 4pi*r^2*|R(r)|^2"
'Locate 4, 5: Print "r in units of a0"
End Sub
'===========================================================
Sub WriteInfo
Color 1, 7
Locate 24, 55: Print "Hydrogen-like orbitals"
Locate 25, 55: Print "Schrodinger equation (1926)"
Locate 26, 55: Print "---------------------------"
Locate 27, 55: Print "Radial: 4*pi*r^2 |R(r)|^2"
Locate 28, 55: Print "Angular: |Y_lm|^2"
Locate 30, 55: Print "Examples:"
Locate 31, 55: Print " 1 0 0 -> 1s"
Locate 32, 55: Print " 2 1 0 -> 2pz"
Locate 33, 55: Print " 2 1 1 -> 2px"
Locate 34, 55: Print " 2 1 -1 -> 2py"
Locate 35, 55: Print " 3 2 0 -> 3dz^2"
End Sub
'===========================================================
Sub DisplayQuantumInfo (n, l, m)
Color 4, 15
Locate 38, 53: Print "Current orbital:"
Locate 39, 53: Print "n ="; n; " l ="; l; " m ="; m
' Orbital name
orbitalName$ = ""
If l = 0 Then orbitalName$ = "s"
If l = 1 Then orbitalName$ = "p"
If l = 2 Then orbitalName$ = "d"
If l = 3 Then orbitalName$ = "f"
mName$ = ""
If l = 0 Then
mName$ = ""
ElseIf l = 1 Then
If m = 0 Then mName$ = "z"
If m = 1 Then mName$ = "x"
If m = -1 Then mName$ = "y"
ElseIf l = 2 Then
If m = 0 Then mName$ = "z^2"
If m = 1 Then mName$ = "xz"
If m = -1 Then mName$ = "yz"
If m = 2 Then mName$ = "x^2-y^2"
If m = -2 Then mName$ = "xy"
End If
Locate 40, 53: Print "Orbital: "; n; orbitalName$; mName$
' Radial nodes
radialNodes = n - l - 1
Locate 41, 53: Print "Radial nodes: "; radialNodes
' Angular nodes
angularNodes = l
Locate 42, 53: Print "Angular nodes: "; angularNodes
End Sub
'===========================================================
Sub PlotRadial (n, l)
x0 = 25
y0 = 320
dr = .25
xscale = 2.5
yscale = 80
' Clear previous plot
Line (15, 335)-(385, 335), 15, BF
Line (15, 15)-(385, 335), 0, B
' Draw axes
Line (x0, 35)-(x0, y0), 2
Line (x0, y0)-(385, y0), 2
' Axis labels
Color 1, 15
Locate 20, 3: Print "0"
Locate 20, 20: Print "5a0"
Locate 20, 35: Print "10a0"
' Draw tick marks
For i = 0 To 10 Step 5
Line (x0 + i * xscale / dr, y0)-(x0 + i * xscale / dr, y0 + 5), 2
Next i
' Calculate and plot radial probability density
maxP = 0
rValueAtMax = 0
' Pre-calculate to find maximum for scaling
r = dr
Do While r < 30
Rnl = RadialFunction(n, l, r)
P = 4 * PI * r * r * Rnl * Rnl
If P > maxP Then
maxP = P
rValueAtMax = r
End If
r = r + dr
Loop
If maxP > 0 Then
yscale = 250 / maxP ' Auto-scale to fit 250 pixels
End If
' Now plot with proper scaling
r = dr
firstPoint = 1
Do While r < 30
Rnl = RadialFunction(n, l, r)
P = 4 * PI * r * r * Rnl * Rnl
xplot = x0 + xscale * (r / dr)
yplot = y0 - yscale * P
' Print xplot, yplot, P, yscale
' Limit y to plot area
If yplot > y0 Then yplot = y0
If firstPoint = 1 Then
PSet (xplot, yplot), 3
firstPoint = 0
Else
If (xplot < 385) Then
Line -(xplot, yplot), 3
End If
End If
r = r + dr
Loop
' Display max value
Color 4, 15
Locate 2, 5: Print "Max P(r) =";
Locate 2, 20: Print Using "##.###"; maxP;
Locate 2, 30: Print "at r =";
Locate 2, 37: Print Using "##.##"; rValueAtMax;
Locate 2, 42: Print "a0"
End Sub
'===========================================================
Function RadialFunction (n, l, r)
' Hydrogen radial wavefunctions R_nl(r)
' Atomic units: a0 = 1
' Normalized so that ∫ r^2 |R|^2 dr = 1
Select Case n
'-------------------------
Case 1 ' 1s
If l = 0 Then
RadialFunction = 2 * Exp(-r)
Else
RadialFunction = 0
End If
'-------------------------
Case 2 ' 2s, 2p
If l = 0 Then
RadialFunction = (1 / Sqr(2)) * (1 - r / 2) * Exp(-r / 2)
ElseIf l = 1 Then
RadialFunction = (1 / (2 * Sqr(6))) * r * Exp(-r / 2)
Else
RadialFunction = 0
End If
'-------------------------
Case 3 ' 3s, 3p, 3d
If l = 0 Then
RadialFunction = (2 / (81 * Sqr(3))) * _
(27 - 18 * r + 2 * r * r) * Exp(-r / 3)
ElseIf l = 1 Then
RadialFunction = (4 / (81 * Sqr(6))) * _
r * (6 - r) * Exp(-r / 3)
ElseIf l = 2 Then
RadialFunction = (4 / (81 * Sqr(30))) * _
r * r * Exp(-r / 3)
Else
RadialFunction = 0
End If
'-------------------------
Case 4 ' 4s, 4p, 4d, 4f
If l = 0 Then ' 4s
RadialFunction = (1 / (768 * Sqr(2))) * _
(192 - 144 * r + 24 * r ^ 2 - r ^ 3) * Exp(-r / 4)
ElseIf l = 1 Then ' 4p
RadialFunction = (1 / (768 * Sqr(6))) * _
r * (80 - 20 * r + r ^ 2) * Exp(-r / 4)
ElseIf l = 2 Then ' 4d
RadialFunction = (1 / (768 * Sqr(30))) * _
r ^ 2 * (12 - r) * Exp(-r / 4)
ElseIf l = 3 Then ' 4f
RadialFunction = (1 / (768 * Sqr(210))) * _
r ^ 3 * Exp(-r / 4)
Else
RadialFunction = 0
End If
'-------------------------
Case Else
RadialFunction = 0
End Select
End Function
'===========================================================
Sub PlotAngularXY (l, m)
cx = 590
cy = 170
R0 = 120
' Clear previous plot
Line (405, 15)-(775, 335), 15, BF
Line (405, 15)-(775, 335), 0, B
' Draw axes
Line (cx - R0, cy)-(cx + R0, cy), 4
Line (cx, cy - R0)-(cx, cy + R0), 4
' Axis labels
Color 4, 15
Locate 3, 74: Print "Y"
Locate 11, 93: Print "X"
theta = 1.57079632679 ' π/2 → XY plane
' --- find max |Ylm|^2 for scaling
maxF2 = 0
For phi = 0 To 6.28318530718 Step 0.034906585
F = Ylm(l, m, theta, phi)
If F * F > maxF2 Then maxF2 = F * F
Next phi
If maxF2 = 0 Then Exit Sub
ANGSCALE = R0 * 0.9 / maxF2
' --- draw multiple isolines
For iso = 0.25 To 1 Step 0.25
firstPoint = 1
For phi = 0 To 6.28318530718 Step 0.034906585
F = Ylm(l, m, theta, phi)
r = ANGSCALE * iso * (F * F)
' +r branch
x1 = cx + r * Cos(phi)
y1 = cy + r * Sin(phi)
' −r branch (critical!)
x2 = cx - r * Cos(phi)
y2 = cy - r * Sin(phi)
If F >= 0 Then
plotColor = 2 ' green
Else
plotColor = 4 ' red
End If
If firstPoint = 1 Then
PSet (x1, y1), plotColor
PSet (x2, y2), plotColor
firstPoint = 0
Else
Line -(x1, y1), plotColor
Line -(x2, y2), plotColor
End If
Next phi
Next iso
' Info text
Color 1, 15
Locate 19, 53: Print "XY plane (theta = 90)"
Locate 20, 53: Print "|Y_lm|^2 isolines"
End Sub
'===========================================================
Sub PlotAngularXZ (l, m)
cx = 200
cy = 520
R0 = 120
'-------------------------------------------------
' Clear plot area
'-------------------------------------------------
Line (15, 355)-(385, 685), 15, BF
Line (15, 355)-(385, 685), 0, B
'-------------------------------------------------
' Draw axes
'-------------------------------------------------
Line (cx - R0, cy)-(cx + R0, cy), 4 ' X
Line (cx, cy - R0)-(cx, cy + R0), 4 ' Z
Color 4, 15
Locate 24, 25: Print "Z"
Locate 33, 45: Print "X"
phi = 0 ' XZ plane
'-------------------------------------------------
' Find max |Y_lm| for scaling
'-------------------------------------------------
maxF = 0
For theta = 0 To 6.28318530718 Step 0.01 ' 0 → 2π
F = Abs(Ylm(l, m, theta, phi))
If F > maxF Then maxF = F
Next theta
If maxF = 0 Then Exit Sub
ANGSCALE = R0 * 0.9 / maxF
'-------------------------------------------------
' Draw isolines of |Y_lm|^2
'-------------------------------------------------
levels = 4
For level = 1 To levels
iso = level / levels
firstPoint = 1
For theta = 0 To 6.28318530718 Step 0.01
F = Ylm(l, m, theta, phi)
' Signed radius → full plane
r = ANGSCALE * iso * F * Abs(F)
x = cx + r * Sin(theta)
y = cy - r * Cos(theta)
If F >= 0 Then
plotColor = 2 + level ' green shades
Else
plotColor = 4 + level ' red shades
End If
If firstPoint = 1 Then
PSet (x, y), plotColor
firstPoint = 0
Else
Line -(x, y), plotColor
End If
Next theta
Next level
'-------------------------------------------------
' Info
'-------------------------------------------------
Color 1, 15
Locate 41, 4: Print "XZ plane (phi = 0)"
' Locate 41, 4: Print "Isolines of |Y_lm|^2"
Locate 42, 4: Print "Angular nodes:"; l
End Sub
'===========================================================
Function Ylm (l, m, theta, phi)
' Real spherical harmonics for hydrogen orbitals
' Normalized real combinations (physics / chemistry convention)
' theta: polar angle [0,pi]
' phi: azimuthal angle [0,2pi]
Dim F As Double
PI = 3.14159265358979
Select Case l
'========================
Case 0 ' s orbital
F = Sqr(1 / (4 * PI))
'========================
Case 1 ' p orbitals
Select Case m
Case 0 ' pz
F = Sqr(3 / (4 * PI)) * Cos(theta)
Case 1 ' px
F = Sqr(3 / (4 * PI)) * Sin(theta) * Cos(phi)
Case -1 ' py
F = Sqr(3 / (4 * PI)) * Sin(theta) * Sin(phi)
Case Else
F = 0
End Select
'========================
Case 2 ' d orbitals
Select Case m
Case 0 ' dz^2
F = Sqr(5 / (16 * PI)) * (3 * Cos(theta) ^ 2 - 1)
Case 1 ' dxz
F = Sqr(15 / (4 * PI)) * Sin(theta) * Cos(theta) * Cos(phi)
Case -1 ' dyz
F = Sqr(15 / (4 * PI)) * Sin(theta) * Cos(theta) * Sin(phi)
Case 2 ' dx^2 - y^2
F = Sqr(15 / (16 * PI)) * Sin(theta) ^ 2 * Cos(2 * phi)
Case -2 ' dxy
F = Sqr(15 / (16 * PI)) * Sin(theta) ^ 2 * Sin(2 * phi)
Case Else
F = 0
End Select
'========================
Case 3 ' f orbitals
Select Case m
Case 0 ' fz^3
F = Sqr(7 / (16 * PI)) * _
(5 * Cos(theta) ^ 3 - 3 * Cos(theta))
Case 1 ' fxz^2
F = Sqr(21 / (64 * PI)) * _
Sin(theta) * (5 * Cos(theta) ^ 2 - 1) * Cos(phi)
Case -1 ' fyz^2
F = Sqr(21 / (64 * PI)) * _
Sin(theta) * (5 * Cos(theta) ^ 2 - 1) * Sin(phi)
Case 2 ' fz(x^2 - y^2)
F = Sqr(105 / (16 * PI)) * _
Sin(theta) ^ 2 * Cos(theta) * Cos(2 * phi)
Case -2 ' fxyz
F = Sqr(105 / (16 * PI)) * _
Sin(theta) ^ 2 * Cos(theta) * Sin(2 * phi)
Case 3 ' fx(x^2 - 3y^2)
F = Sqr(35 / (32 * PI)) * _
Sin(theta) ^ 3 * Cos(3 * phi)
Case -3 ' fy(3x^2 - y^2)
F = Sqr(35 / (32 * PI)) * _
Sin(theta) ^ 3 * Sin(3 * phi)
Case Else
F = 0
End Select
'========================
Case Else
F = 0
End Select
Ylm = F
End Function
Sub PlotAngular3DMeshHidden (l, m, angY, angX)
panelLeft = 405
panelRight = panelLeft + 370
panelTop = 355
panelBottom = 685
panelWidth = panelRight - panelLeft
panelHeight = panelBottom - panelTop
cx = (panelLeft + panelRight) / 2
cy = (panelTop + panelBottom) / 2
alpha = 0
beta = 0
dTheta = .17453293
dPhi = .08726646
' View direction (projection direction)
Vx = -alpha
Vy = -beta
Vz = 1
Vx = 0
Vy = 0
Vz = 1
' --- First pass: compute bounding box ---
minX = 1E+30: maxX = -1E+30
minY = 1E+30: maxY = -1E+30
For theta = 0 To 3.14159265359 Step dTheta
For phi = 0 To 6.28318530718 Step dPhi
Call SurfacePoint(l, m, theta, phi, 350, x, y, z)
' Rotate Y then X
Call RotateY(x, y, z, angY, x1, y1, z1)
Call RotateX(x1, y1, z1, angX, xr, yr, zr)
xs = xr + alpha * zr
ys = yr - beta * zr
If xs < minX Then minX = xs
If xs > maxX Then maxX = xs
If ys < minY Then minY = ys
If ys > maxY Then maxY = ys
Next phi
Next theta
scaleX = panelWidth / (maxX - minX)
scaleY = panelHeight / (maxY - minY)
scaleX = panelWidth / (maxX - minX)
scaleY = panelHeight / (maxY - minY)
scaleF = scaleX
If scaleY < scaleF Then scaleF = scaleY
scaleF = scaleF * .85
centerX3D = (minX + maxX) / 2
centerY3D = (minY + maxY) / 2
Line (panelLeft, panelTop)-(panelRight, panelBottom), 15, BF
Line (panelLeft, panelTop)-(panelRight, panelBottom), 0, B
' --- Second pass: draw with hidden removal ---
For theta = 0 To 3.14159265359 - dTheta Step dTheta
For phi = 0 To 6.28318530718 - dPhi Step dPhi
' --- Compute 3 surface points ---
Call SurfacePoint(l, m, theta, phi, 350, x1, y1, z1)
Call SurfacePoint(l, m, theta + dTheta, phi, 350, x2, y2, z2)
Call SurfacePoint(l, m, theta, phi + dPhi, 350, x3, y3, z3)
' --- Rotate them ---
Call RotateY(x1, y1, z1, angY, x1, y1, z1)
Call RotateX(x1, y1, z1, angX, x1, y1, z1)
Call RotateY(x2, y2, z2, angY, x2, y2, z2)
Call RotateX(x2, y2, z2, angX, x2, y2, z2)
Call RotateY(x3, y3, z3, angY, x3, y3, z3)
Call RotateX(x3, y3, z3, angX, x3, y3, z3)
' --- Compute tangents ---
Tx1 = x2 - x1
Ty1 = y2 - y1
Tz1 = z2 - z1
Tx2 = x3 - x1
Ty2 = y3 - y1
Tz2 = z3 - z1
' --- Normal ---
Nx = Ty1 * Tz2 - Tz1 * Ty2
Ny = Tz1 * Tx2 - Tx1 * Tz2
Nz = Tx1 * Ty2 - Ty1 * Tx2
visibility = Nx * Vx + Ny * Vy + Nz * Vz
If visibility < 0 Then
' --- Projection ---
xs1 = cx + scaleF * (x1 - centerX3D)
ys1 = cy - scaleF * (y1 - centerY3D)
xs2 = cx + scaleF * (x2 - centerX3D)
ys2 = cy - scaleF * (y2 - centerY3D)
xs3 = cx + scaleF * (x3 - centerX3D)
ys3 = cy - scaleF * (y3 - centerY3D)
' --- Depth fading ---
avgZ = (z1 + z2 + z3) / 3
depthColor = 2 + (avgZ + 350) / 700 * 10
If depthColor < 2 Then depthColor = 2
If depthColor > 15 Then depthColor = 15
Line (xs1, ys1)-(xs2, ys2), depthColor
Line (xs1, ys1)-(xs3, ys3), depthColor
End If
Next phi
Next theta
End Sub
Sub SurfacePoint (l, m, theta, phi, R0, x, y, z)
F = Ylm(l, m, theta, phi)
r = R0 * F * F
x = r * Sin(theta) * Cos(phi)
y = r * Sin(theta) * Sin(phi)
z = r * Cos(theta)
End Sub
Sub RotateY (x, y, z, ang, xr, yr, zr)
xr = x * Cos(ang) + z * Sin(ang)
yr = y
zr = -x * Sin(ang) + z * Cos(ang)
End Sub
Sub RotateX (x, y, z, ang, xr, yr, zr)
xr = x
yr = y * Cos(ang) - z * Sin(ang)
zr = y * Sin(ang) + z * Cos(ang)
End Sub
